Hallo,
letzthin war ich zu Beusch bei meiner Mutter im Fränkischen. Gleich hinter der grünen Grenze im Raum Ochsenfurt/Giebelstadt kam ich auf der Landstraße an einem alten Mäuerchen vorbei, das offenbar zum Außenbezirk einer Burgruine gehört. Da muss man natürlich mal anhalten und gucken - das lohnt ja meistens.

Bild 1 Altes einstürzendes Kalksteinmäuerchen, unvermörtelt mit reichlich Nischen.
Erst mal nichts außergewöhnliches auf dem Kalkstubstrat, aber trotzdem immer schön anzusehen:

Bild 2 Protoblastenia rupestris mit seinem olivbraunem Thallus und unberandeten, flachen bis gewölbten, teils knäulig angeordneten, orangen Apothecien. Nicht selten an absonnigen Kalkfelsen.

Bild 3a Eine Diplotomma hedinii mit kräftigem, kreidigem Lager und weiß berandeten, bläulich breiften Apothecien.
Von der ähnliche Art D. alboatrum lässt sie sich am besten durch die Sporen trennen:

Bild 3b Die Sporen sind hier durchweg 4-zellig querseptiert.
Die Art mag es gerne etwas lichtreicher.
Tatsächlich wurde sie an der Ecke der Mauer gefunden, die am weitesten aus dem Wäldchen herausragte.

Bild 4 Pyrenodesmia variabilis ist eine unauffällige, aber bei bei näherer Betrachtung sehr schöne Flechte aus dem Caloplaca-Kreis.
Die weiß berandeten, bläulich bereiften Apothecien über dem braunen Thallus bilden einen hübschen Kontrast.

Bild 5 Die einzeln, rundlich und vulkankraterartig in die Areolen eingesenkten Apothecien verraten Circinaria contorta.
Bei dem Exemplar hier sind die meisten Scheiben kräftig weiß bereift.
Einige Scheiben im gleichen Thallus bleiben hingegen unbereift und erscheinen schwärzlich.
Da der Thallus nicht aus inselartig rundlichen Areolen besteht, sondern eine rissig zusammenhängende Fläche aus eckig-irregulär geformten Feldern bildet, liegt meinem Verständnis nach die Variante C. c. var. hoffmanniana vor.

Bild 6 Placynthium nigrum darf nicht fehlen. Hier Thalli mit gut erkennbarem blaugrünem, radial-fasrigem Prothallus.

Bild 7 Flechtenmosaik mit oranger P. rupestris und brauner L. inundata

Bild 8a In einer regengeschützten Nische eine weißliche Lecanora mit kleinen, bereiften Apothecien.
Der Thallus reagiert R-, aber auffallend UV+grün:

Bild 8b Grüne UV-Fluoreszenz des Lecanora-Thallus. Offenbar etwas aus dem Dunstkreis um Polyozosia albescens / P. pruinosa...
Spannend sind die pyrenocarpen Krusten:

Bild 9a Ockerfarbener bis grünlicher Thallus mit eingesenkten Perithecien auf kompaktem Steinmehl (?), bzw, sehr stark verwittertem Kalkstein.
Ich vermute Schäden durch Schneckenfraß hinter den grünen Bereichen und finde eine Stelle an der Mauer mit sehr unebener Oberfläche (ungünstiger fürs Schneckenzünglein) und einheitlicher Textur:

Bild 9b Verrucaria, die sich als V. viridula einordnen lässt.
"Viridula", da sie im feuchtem Zustand deutlich grüne Algeninseln zeigt.

Bild 9c Weißlicher, stellenweise ockerfarbener Thallus

Bild 9d Schnitt durch Perithecien und Substrat: Ringsum schwarzes Excipulum, vollständig ins Substrat eingesenkt.
Beim Ausfallen tiefe Gruben hinterlassend.
Kleines, apikales Involucrellum.
Große Sporen 26-31 x 16-19 µm, mit ca. 1µm dicker Sporenwand.
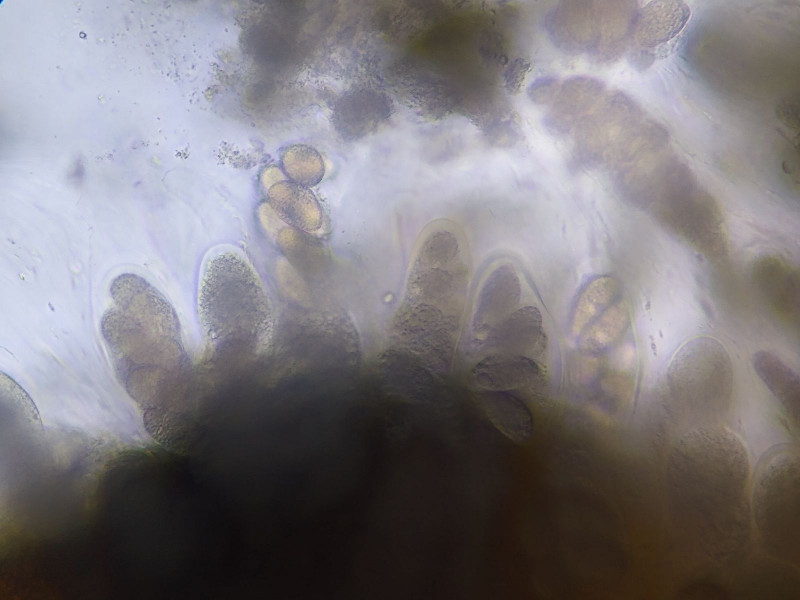
Bild 9e Hymenium mit den für Verrucaria typischen 8-sporigen Asci und großen, elliptischen Sporen.
Auf (vermutlich) derselben Verrucaria befinden sich auch größere, stark gewölbte Perithecien mit Durchmessern bis weit über 0,5 mm.

Bild 10a Großes Perithecium
Tatsächlich sitzen diese dem Thallus relativ lose auf (kippen beim Schneiden leicht um) und weisen auf eine andere Art hin:

Bild 10b Halbkugeliges, schwarzes Involucrellum, innen farblos, algenfrei. Im Zentrum ein kugeliges, dunkeles Excipulum.

Bild 10c Ungewöhnlicher Fruchtkörperbau mit dickem, weißem Bereich zwischen Involucrellum und Excipulum.
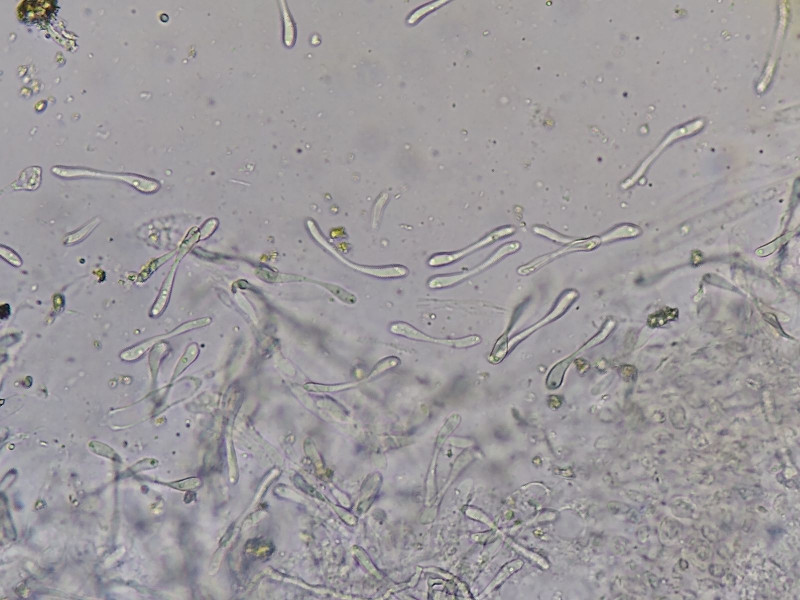
Bild 10d Die Sporen das Fruchtkörpers sind sehr ungewöhnlich: 1-zellig, haylin, lang gestreckt, etwas wellig, hantelförmig, mit verdickten Enden.
Sie messen in Wasser 29,5-36,5 x 3,5-4,5 µm (Breite an der dicksten Stelle bestimmt). 

Bild 10e Asci sind inamyloid, 8-sporig
Hawkworth führt zu Sarcopyrenia gibba var. geisleri, einem lichenicolen Pilz auf diversen Krustenflechtenarten.
Verrucaria wird hier zwar nicht als Wirt erwähnt, die anderen Eigenschaften passen aber sehr gut, insbesondere natürlich die Sporenform.
Die Sporen und andere Mikrobilder / -daten inkl. Schlüssel für die Gattung Sarcopyrenia werden in einer Veröffentlichung von Navarro-Rosinés (2009) gezeigt. Neben diversen Caloplacen, Lecanoren, Aspicilia, Catillaria, Lecania, Protoblastenia wird hier auch Verrucaria (nigrescens) erwähnt, mit denen S. gibba geisleri vergesellschaftet sein kann. Offenbar ist nicht abschließend geklärt, ob der Pilz nur lichenicol oder auch lichenisiert auftreten kann.
Scheinbar ist der Pilz gar nicht selten. Man muss nur die Augen offen halten. Ich bin gespannt, wann ich wieder auf ihn treffe.
LG, Martin


